Synthèse d’amide
Amination des chlorures ou anhydrides d’acyle
Le couplage direct entre un acide carboxylique et une amine n’est pas un choix adapté en chimie de synthèse, en raison de l’échange concomitant de protons entre l’acide et la base. La stratégie la plus courante est la conversion de l’acide en une forme activée (c’est-à-dire plus électrophile), comme le chlorure ou l’anhydride d’acyle. Ces espèces réagissent facilement avec les amines primaires et secondaires pour générer l’amide correspondant.
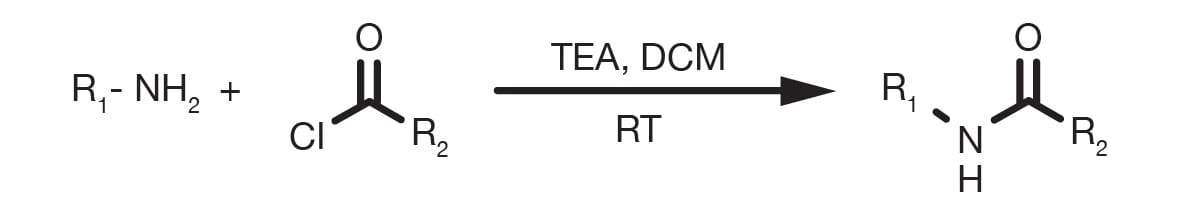
L’acylation de l’amine par le chlorure d’acyle est souvent appelée "réaction de Schotten-Baumann", du nom de ses inventeurs.
La réaction se produit généralement rapidement à température ambiante dans des solvants aprotiques en présence d’une base adaptée, par exemple une amine tertiaire ou de la pyridine. La base en solution aqueuse est souvent ajoutée au goutte-à-goutte, afin de créer à terme un système biphasique.
La réaction de Schotten-Baumann et le couplage entre l’amine et un anhydride sont mécaniquement similaires, la seule différence significative étant le sous-produit de l’acide : de l’HCl pour l’un et un acide carboxylique pour l’autre. Dans les deux cas, une base est requise pour déplacer l’équilibre vers la droite.
La préparation du chlorure d’acyle peut être réalisée in situ en mélangeant l’acide carboxylique avec du chlorure de thionyle ou du chlorure d’oxalyle dans des solvants aprotiques, par exemple du DCM, du THF ou de l’acétate d’éthyle. On obtient normalement de bonnes conversions après quelques heures de reflux du mélange. Il faut isoler le chlorure d’acyle avant l’étape d’amidation avec l’amine.
Méthodes dérivées de chimie peptidique (intermédiaires d’ester actifs)
Des progrès considérables ont été accomplis dans la synthèse des amides au cours des trois dernières décennies, grâce aux travaux réalisés dans le domaine de la synthèse peptidique. Les réactifs de couplage peptidique disponibles sur le marché sont nombreux et variés, mais ils partagent un principe chimique fondamental : la synthèse d’un ester hautement activé. Beaucoup de réactifs de couplage peptidique sont spécialement destinés à la synthèse peptidique automatisée en phase solide ou en solution, mais les mêmes stratégies de synthèse peuvent être utilisées en principe pour la synthèse de n’importe quel amide. Les réactifs les plus courants appartiennent à deux grands groupes :
- Carbodiimmides
- Aminium/uronium d’hydroxybenzotriazole ou sels de phosphonium
Activation au carbodiimide
Les trois réactifs les plus courants pour ce groupe sont le dicyclohéxylcarbodiimide (DCC), le diisopropylcarbodiimide (DIC) et le 1-éthyl-3-(3-diméthylaminopropyl)carbodiimide (EDC). Ils réagissent avec les acides carbonyliques pour former une o-acyl-isourée hautement réactive qui peut être convertie en amide à travers une réaction avec une amine, avec un rendement élevé et un temps de réaction court.
La synthèse de l’o-acyl-isourée bénéficie de l’utilisation de solvants apolaires quand cela est possible (par exemple, du DCM), mais de nombreux solvants aprotiques polaires peuvent également être utilisés.
Les o-acyl-isourées comptent parmi les intermédiaires les plus actifs pour le couplage d’amide, mais ils sont susceptibles de se racémiser spontanément. Cette particularité doit être prise en compte dans la stratégie de synthèse.
C’est également pour cette raison que l’activation de l’acide carboxylique en synthèse peptidique est généralement effectuée en présence d’additifs d’hydroxybenzotriazole qui réagissent rapidement avec l’ester activé. Dans ce cas, l’étape d’activation est mieux décrite comme étant une activation en deux temps au DCC/hydroxybenzotriazole.
Cette deuxième étape de réaction génère un autre ester activé qui ne se racémise pas et qui conserve un niveau d’activation suffisant pour un couplage peptidique efficace.
Les triazoles les plus courants pour cette application sont le 1-hydroxy-benzotriazole (HOBt)et le 1-hydroxy-7-aza-benzotriazole (HOAt).
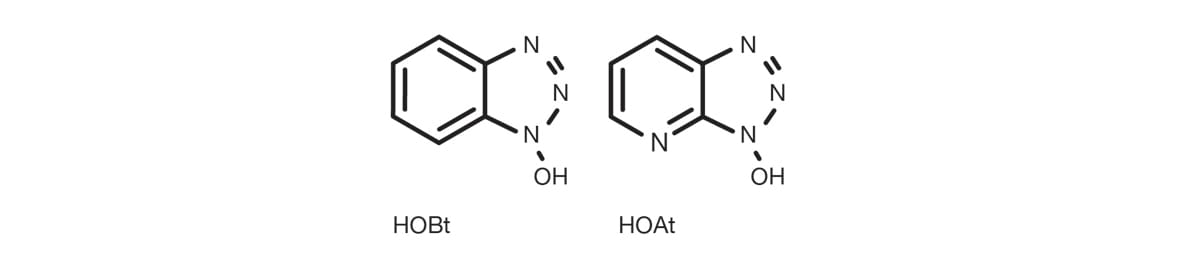
Activation à l’ammonium/uronium et aux sels de phosphonium d’hydroxybenzotriazole
Une stratégie pour éviter le processus d’activation d’acyle en deux temps est possible grâce à l’utilisation d’ammonium/uronium ou de sels de phosphonium des hydroxytriazoles mentionnés ci-dessus. Ainsi, il est possible d’éviter complètement l’utilisation du DCC et la formation de l’intermédiaire o-acyl-isourée.
L’HOBt possède un sel d’uronium correspondant, l’HBTU, et les sels de phosphonium courants associés sont appelés BOP et PyBOP. Les sels d’uronium et de phosphonium correspondants de l’HOAt sont l’HATU et l’AOP/PyAOP, respectivement.
HOBt – HBTU (ou TBTU) – BOP ou PyBOP
HOAt – HATU – AOP ou PyAOP
La réaction directe entre l’acide carboxylique et l’HATU/AOP/PyAOP ou l’HBTU/BOP/PyBOP se produit en présence d’une base (généralement du DIPEA, diisopropyléthylamine) dans des solvants organiques aprotiques polaires, comme le DMF ou l’acétonitrile.
Ces esters activés peuvent être suffisamment couplés à une amine avec des conditions de réaction similaires à celles de la réaction de Schotten-Baumann (base, solvant aprotique, température ambiante).
Protocoles de réaction de référence
Réaction de Schotten-Baumann :
1.
Préparer une solution sous agitation composée de l’amine dans du DCM, ajouter une quantité équimolaire de base (par exemple, DIPEA) suivie de 1 à 2 équivalents du chlorure d’acyle. Agiter à température ambiante pendant 8 à 16 heures. La réaction est normalement neutralisée à l’eau et extraite avec du DCM ou d’autres solvants organiques en fonction des caractéristiques de l’amide.
2.
Préparer la solution d’amine et de base (équimolaire) à 0°C. Refroidir le mélange sous des conditions d’agitation à -75°C, puis ajouter le chlorure d’acyle. Agiter pendant 1 à 6 h, puis neutraliser à l’eau, extraire avec du DCM et procéder à la purification du produit.
Méthode de carbodiimmide :
Préparer une solution d’acide dans du DMF et ajouter 2 ou 3 équivalents de base. Refroidir la solution à 0°C et ajouter 2 équivalents de DCC ou d’EDC. Agiter à température ambiante pendant 30 à 60 minutes, puis diluer à l’eau et extraire avec un solvant organique en fonction des propriétés du produit de l’amide. Procéder à la purification du produit.
HATU/HBTU
Préparer une solution d’acide dans du DMF à 0°C, puis ajouter 2 équivalents de HATU (550 mg, 1,4 mmol) et 3 équivalents de base (par exemple, DIPEA ou TEA). Enfin, ajouter un léger excédent d’amine (par rapport à l’acide) et agiter à température ambiante pendant 30 à 60 minutes. Diluer à l’eau et extraire avec un solvant organique en fonction des propriétés du produit de l’amide. Procéder à la purification du produit.
Le protocole de référence reste le même quand d’autres activateurs sont utilisés, par exemple l’AOP, le PyBOP, le BOP, etc.
En cas d’utilisation de l’HBTU, le protocole reste similaire, mais il est souvent nécessaire d’augmenter la température de la réaction et certains auteurs ont signalé des conditions de reflux et des temps de conversion légèrement plus longs, jusqu’à 2 ou 3 heures.
Utilisation combinée du carbodiimmide et de l’hydroxybenzotriazole
Préparer une solution d’acide (700 mg, 3,2 mmol) dans du DMF (10 mL), ajouter 3 équivalents de base (par exemple, DIPEA, NH4Cl ou TEA) tout en refroidissant la réaction à 0°C. Traiter le mélange avec 2 équivalents d’éthylcarbodiimide (ou autre carbodiimmide) et 2 équivalents d’HOBt (ou HOAt). Enfin, ajouter 1,5 équivalent d’amine. Agiter à température ambiante pendant 30 à 60 minutes. Neutraliser à l’eau et extraire avec un solvant organique en fonction des propriétés du produit de l’amide. Procéder à la purification du produit.
Exemples
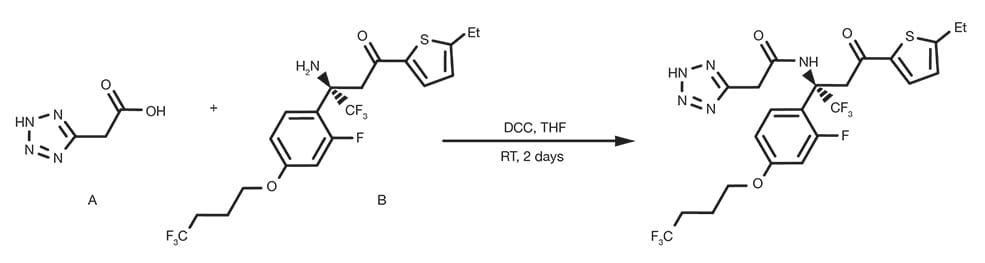
Référence de brevet : WO2015191681

Référence de brevet : WO2015129926
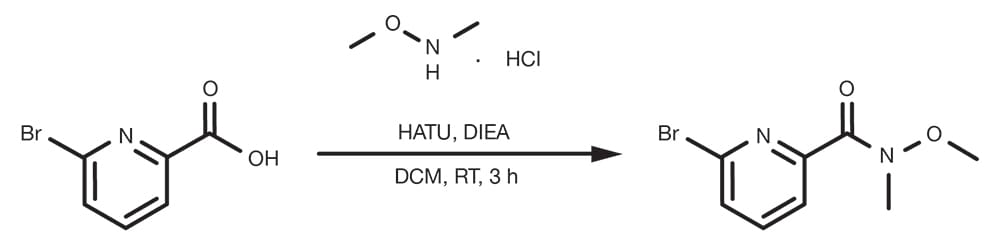
Référence de brevet : WO2015140133
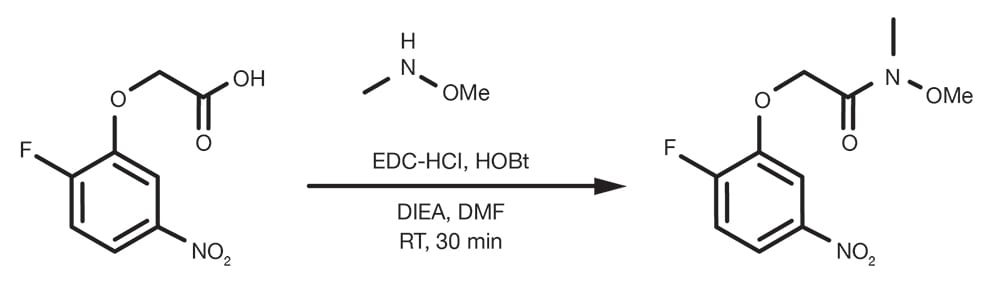
Référence de brevet : WO2014149164
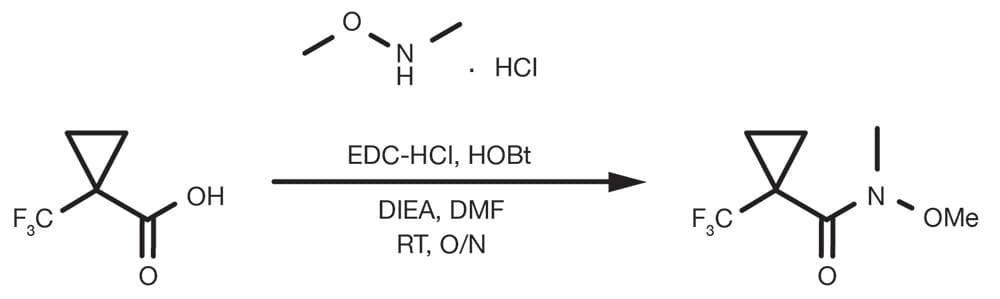
Référence de brevet : WO2015129926
Publications de référence clés
- Schotten, C. Berichte der deutschen chemischen Gesellschaft. 1884, 17, 2544. doi:10.1002/cber.188401702178.
- Baumann, E. Berichte der deutschen chemischen Gesellschaft. 1886, 19, 3218. doi:10.1002/cber.188601902348.
- Emil Fischer Berichte der deutschen chemischen Gesellschaft. 1903, 36, 2982–2992. doi:10.1002/cber.19030360356.
- Jaradat, Da’san M. M. "Thirteen decades of peptide synthesis: key developments in solid phase peptide synthesis and amide bond formation utilized in peptide ligation". Amino Acids. 2017, 50 (1): 39–68. doi:10.1007/s00726-017-2516-0. ISSN 0939-4451
- El-Faham A, Albericio F. "Peptide coupling reagents, more than a letter soup". Chemical Reviews. 2011, 111, 6557–602. doi:10.1021/cr100048w
Choix de produits
Solvants :
Traitement conclusif :
VOIR TOUS NOS SOLVANTS – PLUS DE 1 000 ALTERNATIVES
Ingrédients/additifs basiques :
Traitement conclusif :
UTILISEZ LA BARRE DE RECHERCHE EN HAUT DE LA PAGE POUR LANCER UNE RECHERCHE PAR NOM DE PRODUIT OU PAR NUMÉRO CAS
Agents d’activation :
Dicyclohéxylcarbodiimide (DCC)
1-éthyl-3-(3-diméthylaminopropyl)carbodiimide (EDC)
1-hydroxy-benzotriazole (HOBt)
Hexafluorophosphate de N,N,N’,N’-tétraméthyl-O-(1H-benzotriazol-1-yl)uronium
Hexafluorophosphate d’o-(benzotriazol-1-yl)-N,N,N’,N’-tétraméthyluronium (HBTU)
Hexafluorophosphate de (benzotriazol-1-yloxy)tris(diméthylamino)phosphonium (BOP)
Hexafluorophosphate de (benzotriazol-1-yloxy)tripyrrolidinophosphonium (PyBOP)
Hexafluorophosphate de tris(diméthylamino)(3H-1,2,3-triazolo[4,5-b]pyridin-3-yloxy)phosphore (AOP)
Hexafluorophosphate de (7-azabenzotriazol-1-yloxy)tripyrrolidinophosphonium (PyAOP)
Blocs de construction :
Chlorures d'alkyle ou d'acyle (het) aromatiques:
Chlorure d'isoxazole-5-carbonyle
Acides carboxyliques d'alkyle ou (hét) aromatiques:
Acide 3,5-diméthoxy-4-méthylbenzoïque
Autres acides carboxyliques (plus de 5000 articles)
Alkylnitriles (amides provenant de l'hydrolyse du nitrile):
Cétones cycliques saturées (pour l’amidation de Sheppard donner des lactames):
N- (éthoxycarbonyl) nortropinone
Aryl alkyl cétones:
Ammoniac (solution dans le méthanol)
Amines:






